Diferenças entre edições de "PV"
m |
|||
| Linha 2: | Linha 2: | ||
==Introdução teórica== | ==Introdução teórica== | ||
| − | + | Nesta experiência vamos estudar um dos fenómenos particular da lei dos gases perfeitos: a Lei de Boyle-Mariotte, onde se constata que a pressão e o volume de um gás são inversamente proporcionais mantida a temperatura fixa, ou seja: | |
| − | PV = constante | + | PV = constante = nRT |
| − | Esta relação matemática diz-nos que num gás perfeiro | + | Esta relação matemática diz-nos que num gás perfeiro quando diminuimos o volume, a pressão a que o gás está sujeito aumenta. |
| + | |||
| + | Para realizar a experiência necessitaremos de construir um manómetro para determinar a pressão uma vez que o vulome pode ser determinado por uma medida direta como veremos. | ||
(foto de um manómetro) | (foto de um manómetro) | ||
| − | Um manómetro é instrumento que mede a pressão de gases ou líquidos | + | Um manómetro é instrumento que mede a pressão de gases ou líquidos. Para pressões baixas e proximas da atmosfera poderemos construir um manómetro simples recorrendo a uma simples coluna de água. |
| − | |||
==A experiência em casa== | ==A experiência em casa== | ||
Os ingredientes para esta experiência são: | Os ingredientes para esta experiência são: | ||
| − | * Uma seringa | + | * Uma seringa de 100 ml |
| − | * Um tubo transparente | + | * Um tubo plástico flexivel transparente com diametro interior de 4 mm |
| − | * Água qb | + | * Água qb |
| + | * Corante alimentar | ||
| + | * Fita métrica | ||
| + | * Suporte | ||
| + | |||
| + | Coloca-se o tubo numa configuração em U e enche-se a meia-altura com a água previamente misturada com um pouco de corante. Une-se a seringa ao tubo, de maneira a que não haja fugas na ligação, podendo usar-se uma cola vulgar de PVC. A seringa deve estar com o êmbolo expandido mas não no fim de escala (~90ml). | ||
| + | |||
| + | De seguida determina-se para vários valores do volume da seringa (ex. 80 ml a 100 ml) o diferencial na altura das duas colunas de água. Deve-se varrer várias vezes o volume de modo a poder concluir sobre o erro experimental. | ||
| + | O comprimento do tudo ligado à seringa com ar permite calcular o volume total de ar pela adição com o volume da seringa. | ||
| + | A diferença entre a altura do liquido permite estabelecer o valor da pressão pela fórmula: | ||
| − | + | <math>P_h= \mu gh=K.h</math> | |
| − | + | onde a constante K é de 9800 Pa/m ou 9,8 Pa/mm. | |
==A experiência no e-lab== | ==A experiência no e-lab== | ||
Revisão das 10h45min de 5 de janeiro de 2016
Navegação: Mysolutions > MOOC FEX > PV
Introdução teórica
Nesta experiência vamos estudar um dos fenómenos particular da lei dos gases perfeitos: a Lei de Boyle-Mariotte, onde se constata que a pressão e o volume de um gás são inversamente proporcionais mantida a temperatura fixa, ou seja:
PV = constante = nRT
Esta relação matemática diz-nos que num gás perfeiro quando diminuimos o volume, a pressão a que o gás está sujeito aumenta.
Para realizar a experiência necessitaremos de construir um manómetro para determinar a pressão uma vez que o vulome pode ser determinado por uma medida direta como veremos.
(foto de um manómetro)
Um manómetro é instrumento que mede a pressão de gases ou líquidos. Para pressões baixas e proximas da atmosfera poderemos construir um manómetro simples recorrendo a uma simples coluna de água.
A experiência em casa
Os ingredientes para esta experiência são:
- Uma seringa de 100 ml
- Um tubo plástico flexivel transparente com diametro interior de 4 mm
- Água qb
- Corante alimentar
- Fita métrica
- Suporte
Coloca-se o tubo numa configuração em U e enche-se a meia-altura com a água previamente misturada com um pouco de corante. Une-se a seringa ao tubo, de maneira a que não haja fugas na ligação, podendo usar-se uma cola vulgar de PVC. A seringa deve estar com o êmbolo expandido mas não no fim de escala (~90ml).
De seguida determina-se para vários valores do volume da seringa (ex. 80 ml a 100 ml) o diferencial na altura das duas colunas de água. Deve-se varrer várias vezes o volume de modo a poder concluir sobre o erro experimental. O comprimento do tudo ligado à seringa com ar permite calcular o volume total de ar pela adição com o volume da seringa. A diferença entre a altura do liquido permite estabelecer o valor da pressão pela fórmula:
[math]P_h= \mu gh=K.h[/math]
onde a constante K é de 9800 Pa/m ou 9,8 Pa/mm.
A experiência no e-lab
A experiência do e-lab é semelhante à que é feita em casa, excepto que em vez de água para medir o deslovamen-to/volume, aqui usamos um sensor para medir a pressão com mais precisão. A montagem consiste num cilindro cheio de ar, cujo êmbolo é movido por um pequeno motor electrico. O par cilindro / êmbolo é implementado com uma seringa de 5cc.
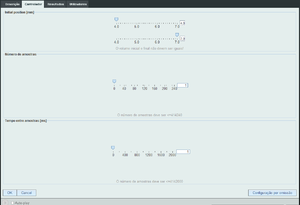
Na sala de controlo podemos escolher os volumes inicial e final. Há que notar que podemos correr a experiência como compressão ou expansão. O tempo entre aquisições permite-nos controlar o tempo da experiência. É importante prestar atenção a isto, pois o a lei em estudo só é válida para transformações adiabáticas.
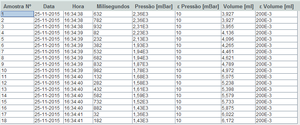
No final, obtemos uma tabela de resultados em que cada linha corresponde a uma amostra. As colunas que nos interessam são a pressão e o volume.
Podemos apresenta-los graficamente:
(Fazer o plot dos dados no excel ou no fitteia)
Podemos representar estes dados na forma de gráfico. Imediatamente vemos uma relação 1/x. Podemos fazer directamen-te o ajuste a esta função.
(fazer o ajuste)
Para além disso, podemos também estudar a constante dos gases perfeitos. R = P*V / n*T