Diferenças entre edições de "Gás ideal em processos quase estáticos"
Saltar para a navegação
Saltar para a pesquisa
(Criou a página com "Misturam-se 2 g de He com 4 g de O<sub>2</sub> à temperatura ambiente. Considere estes gases como ideais. a) Calcule a quantidade de calor \( Q \) que é preciso fornecer...") |
|||
| Linha 1: | Linha 1: | ||
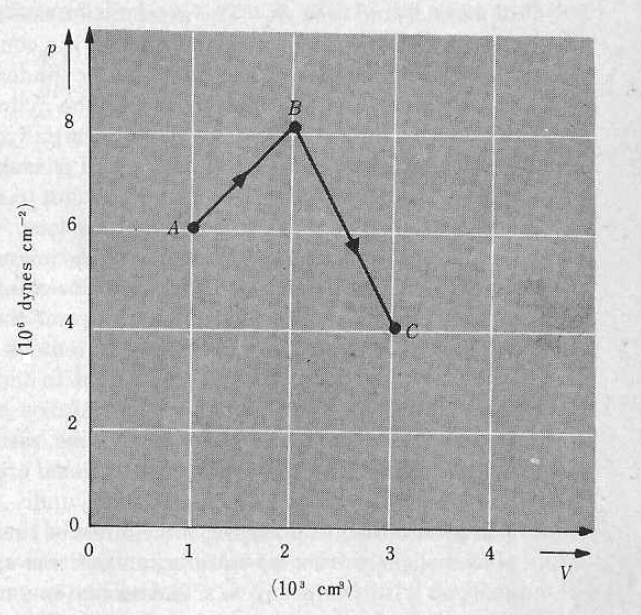
| − | + | Uma mole de um gás ideal diatómico é sujeita ao processo quase estático \( A \rightarrow B \rightarrow C \) ilustrado no diagrama que se apresenta na figura. Determine: | |
| − | a) | + | a) O calor específico por mole a volume constante, \( c_V \), do gás. |
| − | b) | + | b) O trabalho \( W \) realizado pelo gás neste processo. |
| − | c) | + | c) O calor \( Q \) absorvido pelo gás neste processo. |
| − | + | ||
| − | + | [[Ficheiro:3.png|200px|left|frame|]] | |
| − | |||
<div class="toccolours mw-collapsible mw-collapsed" style="width:210px"> | <div class="toccolours mw-collapsible mw-collapsed" style="width:210px"> | ||
'''Respostas''' | '''Respostas''' | ||
<div class="mw-collapsible-content"> | <div class="mw-collapsible-content"> | ||
| − | a) \( | + | a) \( c_V \simeq 20,78 \) J mol<sup>-1</sup> K<sup>-1</sup> |
| − | b) \( | + | b) \( W = 1300 \) J |
| − | c) \( Q | + | c) \( Q = 2800 \) J |
</div> | </div> | ||
</div> | </div> | ||
| Linha 33: | Linha 32: | ||
*AUTOR: | *AUTOR: | ||
*MATERIA PRINCIPAL: Teoria cinética dos gases | *MATERIA PRINCIPAL: Teoria cinética dos gases | ||
| − | *DESCRICAO: | + | *DESCRICAO: Gás ideal em processos quase estáticos |
*DIFICULDADE: ** | *DIFICULDADE: ** | ||
| − | *TEMPO MEDIO DE RESOLUCAO: | + | *TEMPO MEDIO DE RESOLUCAO: 1200 [s] |
| − | *TEMPO MAXIMO DE RESOLUCAO: | + | *TEMPO MAXIMO DE RESOLUCAO: 1800 [s] |
| − | *PALAVRAS CHAVE: Calor específico a volume e a pressão constante | + | *PALAVRAS CHAVE: O gás perfeito, Calor específico a volume e a pressão constante |
</div> | </div> | ||
</div> | </div> | ||
Revisão das 14h31min de 27 de dezembro de 2015
Uma mole de um gás ideal diatómico é sujeita ao processo quase estático \( A \rightarrow B \rightarrow C \) ilustrado no diagrama que se apresenta na figura. Determine:
a) O calor específico por mole a volume constante, \( c_V \), do gás.
b) O trabalho \( W \) realizado pelo gás neste processo.
c) O calor \( Q \) absorvido pelo gás neste processo.
Respostas
a) \( c_V \simeq 20,78 \) J mol-1 K-1
b) \( W = 1300 \) J
c) \( Q = 2800 \) J
Metadata
- CONTEXTO : Primeiro ciclo universitário
- AREA: Física
- DISCIPLINA: Termodinâmica e Estrutura da Matéria
- ANO: 2
- LINGUA: pt
- AUTOR:
- MATERIA PRINCIPAL: Teoria cinética dos gases
- DESCRICAO: Gás ideal em processos quase estáticos
- DIFICULDADE: **
- TEMPO MEDIO DE RESOLUCAO: 1200 [s]
- TEMPO MAXIMO DE RESOLUCAO: 1800 [s]
- PALAVRAS CHAVE: O gás perfeito, Calor específico a volume e a pressão constante